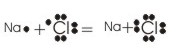Lilith
MFC Üyesi
- Üyelik Tarihi
- 5 Ağu 2017
- Konular
- 310
- Mesajlar
- 1,083
- MFC Puanı
- 120
MADDENİN TEMEL ÖZELLİKLERİ
KİMYA : Maddenin yapısını ve maddeler arasındaki ilişkiyi inceleyen pozitif bir bilimdir.
MADDE : Hacmi ve kütlesi olan her varlık maddedir. "Taş, hava, su, ağaç... vb. gibi."
MADDENİN ORTAK ÖZELLİKLERİ : Her maddede olması gereken özelliklere ortak özelliklere denir. Bunları şöyle sıralayabiliriz.
1) Kütle : Evrendeki madde miktarıdır.
2) Hacim : Madde miktarının uzayda doldurduğu boşluktur.
3) Eylemsizlik : Maddenin sahip olduğu durumu koruma isteğidir.
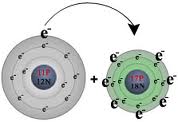
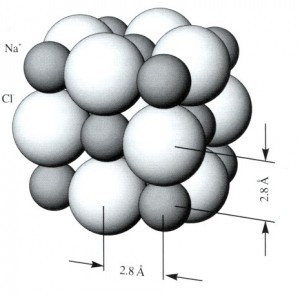
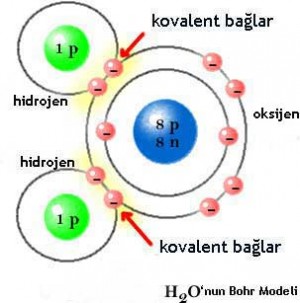
4)Tanecikli Yapı:Bütün maddeler atom denilen küçük taneciklerden yapılmıştır.Atomlar da proton,nötron ve elektron gibi küçük taneciklerden yapılmıştır. Bütün bu tanecikler arasında boşluklar vardır. Onun için madenin yapısında boşluklu ve tanecikli yapı esastır.
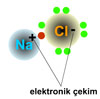
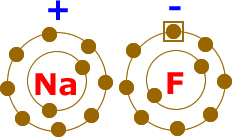
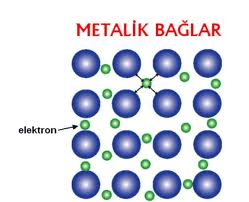
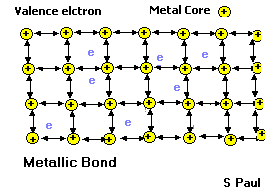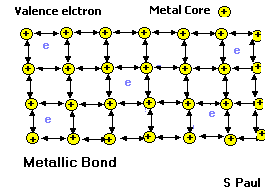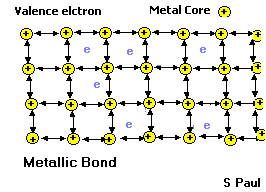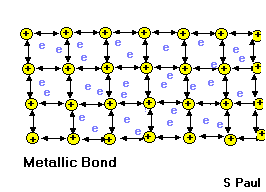
5) Elektrikli Yapı: Bütün maddelerin yapısında + ve - yükler mevcuttur. Bunlardan biri eksik olursa madde madde olmaktan çıkar.
KİMYA : Maddenin yapısını ve maddeler arasındaki ilişkiyi inceleyen pozitif bir bilimdir.
MADDE : Hacmi ve kütlesi olan her varlık maddedir. "Taş, hava, su, ağaç... vb. gibi."
MADDENİN ORTAK ÖZELLİKLERİ : Her maddede olması gereken özelliklere ortak özelliklere denir. Bunları şöyle sıralayabiliriz.
1) Kütle : Evrendeki madde miktarıdır.
2) Hacim : Madde miktarının uzayda doldurduğu boşluktur.
3) Eylemsizlik : Maddenin sahip olduğu durumu koruma isteğidir.
4)Tanecikli Yapı:Bütün maddeler atom denilen küçük taneciklerden yapılmıştır.Atomlar da proton,nötron ve elektron gibi küçük taneciklerden yapılmıştır. Bütün bu tanecikler arasında boşluklar vardır. Onun için madenin yapısında boşluklu ve tanecikli yapı esastır.
5) Elektrikli Yapı: Bütün maddelerin yapısında + ve - yükler mevcuttur. Bunlardan biri eksik olursa madde madde olmaktan çıkar.