OBERON
MFC Üyesi
-
- Üyelik Tarihi
- 20 Kas 2016
-
- Mesajlar
- 3,156
-
- MFC Puanı
- 41
Orbital, elektronların atom çekirdeği etrafındaki yörüngelerde (Enerji seviyelerinde) bulunma olasılığının en fazla olduğu hacimsel bölgelere denir.Fizikte atomik, kimyada orbital olarak geçer.
Bir yörüngede kaç orbital bulunduğunu hesaplamak için n2 parametresi kullanılır. n, burada "yörünge numarası" veya "Baş kuantum sayısı" adıyla anılır.
II. Molekül Orbitali :Bir molekül üzerinde tamamen dağılmış olduğu düşünülen atomik orbitallerle aynı matematiksel özelliklere sahip olan matematiksel fonksiyonlardır. Psi ile simgelenir. Örnek: sigma,pi,delta orbitalleri.
Molekül Orbital teorisine göre moleküller meydana gelirken, atomlar gerekli bağ mesafesinde birbirlerine yaklaştıklarında molekül oluşmadan önce atomlarda bulunan atomik orbitaller karışarak moleküle ait orbitalleri olusturular. Bu nedenle molekül oluştuktan sonra atomik orbitallerden bahsedilemez.
Atomik orbitallerin karışması molekül orbital teorisinin temeli olup, uygun simetri ve enerjide ancak molekül orbitallerini olusturabilirler. Molekül orbital diyagramları ise atomik orbitallerin molekül orbitallerini oluşturmak üzere nasıl birleştikleri gösteren diyagramlardır.
Elektronların orbitallere dağılımı
Bir orbitalde en fazla iki elektron bulunabilir.
Örnek:
Neon atomunun elektron dizilimi şöyledir: 1s2, 2s2, 2p6
Neon atomunun Orbital şeması ise şöyledir:
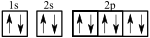
Hund kuralı
Aynı temel enerji düzeyindeki eş enerjili orbitallere elektronlar önce birer birer yerleşir. Daha sonra tekrar başa dönerek ikinci elektronlar yerleşir. Bu kurala Hund kuralı denir.
Örnek:
Karbon atomunun elektron dizilimi şöyledir: 1s2, 2s2, 2p2.
Karbon atomunun Orbital şeması ise şöyledir:

Bir yörüngede kaç orbital bulunduğunu hesaplamak için n2 parametresi kullanılır. n, burada "yörünge numarası" veya "Baş kuantum sayısı" adıyla anılır.
II. Molekül Orbitali :Bir molekül üzerinde tamamen dağılmış olduğu düşünülen atomik orbitallerle aynı matematiksel özelliklere sahip olan matematiksel fonksiyonlardır. Psi ile simgelenir. Örnek: sigma,pi,delta orbitalleri.
Molekül Orbital teorisine göre moleküller meydana gelirken, atomlar gerekli bağ mesafesinde birbirlerine yaklaştıklarında molekül oluşmadan önce atomlarda bulunan atomik orbitaller karışarak moleküle ait orbitalleri olusturular. Bu nedenle molekül oluştuktan sonra atomik orbitallerden bahsedilemez.
Atomik orbitallerin karışması molekül orbital teorisinin temeli olup, uygun simetri ve enerjide ancak molekül orbitallerini olusturabilirler. Molekül orbital diyagramları ise atomik orbitallerin molekül orbitallerini oluşturmak üzere nasıl birleştikleri gösteren diyagramlardır.
Elektronların orbitallere dağılımı
Bir orbitalde en fazla iki elektron bulunabilir.
Örnek:
Neon atomunun elektron dizilimi şöyledir: 1s2, 2s2, 2p6
Neon atomunun Orbital şeması ise şöyledir:

Hund kuralı
Aynı temel enerji düzeyindeki eş enerjili orbitallere elektronlar önce birer birer yerleşir. Daha sonra tekrar başa dönerek ikinci elektronlar yerleşir. Bu kurala Hund kuralı denir.
Örnek:
Karbon atomunun elektron dizilimi şöyledir: 1s2, 2s2, 2p2.
Karbon atomunun Orbital şeması ise şöyledir:
